
Points clés à retenir
- AstraZeneca a suspendu les essais cliniques de phase 3 des vaccins COVID-19 dans le monde.
- Un participant à un essai clinique au Royaume-Uni aurait souffert d'un trouble inflammatoire de la colonne vertébrale.
- Un comité d'experts indépendants étudie la maladie et déterminera quand les essais cliniques de phase 3 pourront reprendre.
MISE À JOUR: Depuis le 23 octobre, AstraZeneca a repris les essais de vaccins aux États-Unis.Les essais cliniques de la société ont repris pour la première fois au Royaume-Uni le 12 septembre.
La société pharmaceutique AstraZeneca a suspendu les essais cliniques humains de stade avancé des vaccins COVID-19 dans le monde le 9 septembre après qu'un participant au Royaume-Uni soit tombé malade.
Le patient peut avoir développé une inflammation de la moelle épinière appelée myélite transverse, mais les détails n'ont pas été officiellement publiés. On ne sait pas si la personne qui est tombée malade a reçu le vaccin ou un placebo, bien que STAT ait déclaré avoir reçu le vaccin.
À présent, un comité d'experts indépendants mandaté par AstraZeneca examine les données de sécurité entourant l'événement, qui est le protocole des grands essais cliniques lorsqu'une maladie inattendue ou inexpliquée survient chez un participant.
«Nous serons guidés par ce comité quant au moment où les essais pourraient redémarrer, afin de pouvoir poursuivre notre travail le plus tôt possible pour fournir ce vaccin de manière large, équitable et sans profit pendant cette pandémie», Pascal Soriot, Directeur général d'AstraZeneca, a déclaré dans un communiqué.
Le monde regarde et attend un vaccin COVID-19, donc entendre qu'il y a une pause peut être décourageant. La bonne nouvelle est que cela signifie que les chercheurs suivent le processus scientifique plutôt que de succomber à la pression politique pour produire rapidement un vaccin.
Ce que cela signifie pour vous
Bien que les essais cliniques soient suspendus, ils ne sont pas terminés. L'espoir n'est pas perdu qu'un vaccin COVID-19 deviendra disponible à l'avenir. Les chercheurs de neuf sociétés pharmaceutiques travaillent ensemble et suivent des protocoles pour garantir qu'un vaccin COVID-19 sûr et efficace sera finalement approuvé, fabriqué et mis à la disposition du public.
Que signifie une pause?
La pause dans les essais cliniques de phase 3 ne signifie pas qu’il n’y aura jamais de vaccin contre le SRAS-CoV-2 - le virus qui cause le COVID-19 - et que nous ne pourrons jamais quitter nos maisons. La pause garantit qu'un processus d'examen standard est en cours pour sauvegarder l'intégrité des neuf essais cliniques de phase 3 actuellement en cours pour un vaccin COVID-19.
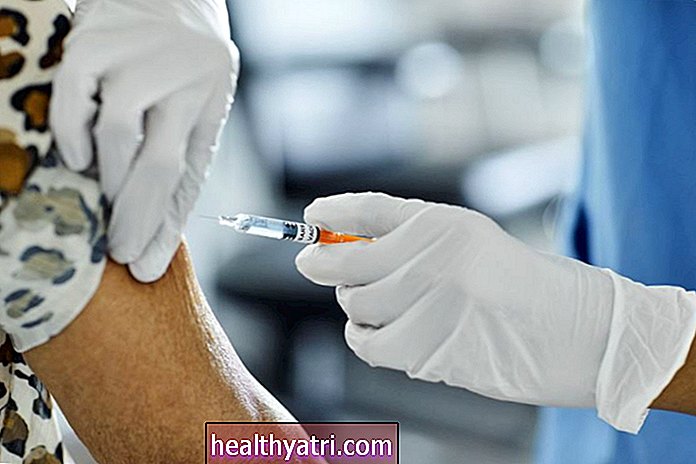
Au cours des essais cliniques, des effets secondaires légers sont attendus, tels que des douleurs au site d'injection, des maux de tête et de la fatigue. Chacun de ces effets secondaires peut être un signe que le système immunitaire réagit et crée des anticorps. Mais des symptômes comme les maux de tête et la fatigue surviennent avec de nombreuses maladies et peuvent être des événements fortuits chez les personnes participant à des essais cliniques. Ces effets secondaires bénins ne sont pas alarmants.
Lorsque des effets secondaires inattendus ou une maladie plus grave surviennent chez un participant de phase 3, les scientifiques suspendent temporairement un essai clinique jusqu'à ce qu'ils enquêtent sur la situation.
Alors que l'essai AstraZeneca est suspendu, huit autres sociétés sont au milieu d'essais cliniques de phase 3, selon leNew York Timestraqueur de vaccin contre le coronavirus:
- BioNTech
- GlaxoSmithKline
- Johnson & Johnson
- Merck
- Moderna
- Novavax
- Pfizer
- Sanofi
Quel est le processus de développement d'un nouveau vaccin?
Le processus de création d'un nouveau vaccin comporte six étapes, selon les Centers for Disease Control and Prevention (CDC). Les deux premières étapes impliquent l'exploration et une étape préclinique, au cours de laquelle les scientifiques effectuent des travaux de laboratoire et commencent à étudier les effets d'un vaccin nouvellement créé sur les cellules et les animaux. La troisième étape est le développement clinique, qui comprend trois phases:
- Phase 1: Au cours d'une étude de phase 1, les scientifiques tentent de déterminer la dose de vaccin la plus forte qui cause le moins d'effets secondaires. Cela aide à déterminer la dose appropriée à administrer aux personnes. Quelques dizaines de personnes participent aux études de phase 1.
- Phase 2. Dans une étude de phase 2, le vaccin est testé sur des centaines de personnes présentant des caractéristiques similaires, telles que l'âge, le sexe et les conditions médicales, afin de déterminer l'efficacité du vaccin chez certains types de personnes. Si les études de phase 2 réussissent, les gens produiront des anticorps et l'essai clinique passera à la phase 3.
- Phase 3. Le but des essais cliniques de phase 3 est d'évaluer l'innocuité d'un vaccin. Des milliers de personnes participent aux essais de phase 3 et les scientifiques continuent de surveiller l'efficacité du vaccin, ainsi que les effets secondaires que les gens ressentent.
Vaccins COVID-19: Restez à jour sur les vaccins disponibles, qui peut les obtenir et leur sécurité.
Prochaines étapes
Une fois les essais cliniques de phase 3 redémarrés, ils se poursuivront jusqu'à ce qu'il y ait suffisamment de preuves de l'innocuité et de l'efficacité du vaccin. Ensuite, la quatrième étape du processus de développement du vaccin peut avoir lieu: le vaccin est transmis à la Food and Drug Administration (FDA) pour examen et approbation réglementaires.
Lorsque le vaccin est approuvé, la cinquième étape peut se dérouler: le vaccin commence à être fabriqué et distribué. Les tests ne s'arrêtent cependant pas là. Des tests de contrôle qualité sont effectués tout au long du processus de fabrication et les installations de fabrication sont inspectées par la FDA. Des études pour surveiller les effets secondaires (également appelés événements indésirables) chez les personnes vaccinées ont lieu après l'approbation, l'homologation et l'administration du vaccin au public.
Pour l’instant, nous attendons que le comité d’experts indépendants d’AstraZeneca procède à son examen. Nous continuons à nous laver les mains, à porter nos masques et à rester à six pieds l'un de l'autre pour faire ce que nous pouvons pour prévenir ou ralentir la propagation du SRAS-CoV-2.
Comment les vaccins COVID-19 fonctionneront-ils?
Il existe plusieurs variantes de vaccins COVID-19 dans les tests de phase 3, mais tous doivent transmettre une infime partie du virus SARS-CoV-2 dans votre corps. Le tout petit peu de matériel génétique n'est pas suffisant pour vous rendre malade, mais juste assez pour que votre système immunitaire puisse le reconnaître comme un matériau étranger et créer des anticorps contre lui. Cette réponse prépare votre système immunitaire de sorte que si vous entrez en contact avec le SRAS-CoV-2 à l'avenir, votre corps puisse l'attaquer immédiatement, empêchant une maladie à part entière.







-test-for-hcv.jpg)

-side-effects.jpg)



.jpg)



-hearing-tests.jpg)

