Points clés à retenir
- La Food and Drug Administration (FDA) a délivré une autorisation d'utilisation d'urgence (EUA) d'un traitement aux anticorps contre le coronavirus fabriqué par Eli Lilly.
- Le cocktail d'anticorps est appelé bamlanivimab et son utilisation a été autorisée chez les patients à haut risque récemment diagnostiqués de 12 ans et plus.
- Eli Lilly a déclaré qu'il prévoyait de fabriquer jusqu'à un million de doses de bamlanivimab d'ici la fin de 2020.
La Food and Drug Administration (FDA) a annoncé lundi dans une lettre qu'elle délivrerait une autorisation d'utilisation d'urgence (EUA) d'un traitement par anticorps neutralisant COVID-19 fabriqué par la société pharmaceutique Eli Lilly.
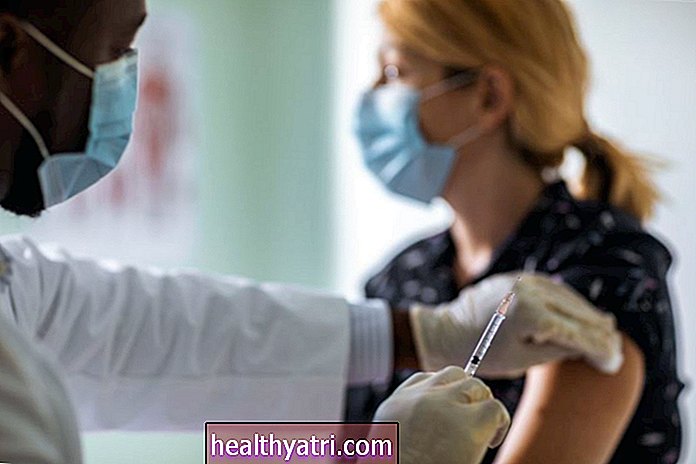
"Cette autorisation d'urgence nous permet de mettre à disposition un traitement COVID-19 pour les patients récemment diagnostiqués à haut risque - en ajoutant un outil précieux pour les médecins qui luttent contre le fardeau de plus en plus lourd de cette pandémie mondiale", Dave Ricks, président-directeur général d'Eli Lilly, a déclaré dans un communiqué de presse.
La possibilité d'un traitement viable survient à un moment où le COVID-19 infecte plus de 140 000 personnes par jour.
Le traitement, appelé bamlanivimab (LY-CoV555), a été autorisé pour le traitement du COVID-19 d'intensité légère à modérée chez les adultes et les enfants de 12 ans et plus avec un test COVID-19 positif et qui présentent un risque élevé d'évolution vers sévère. COVID-19 et / ou hospitalisation, selon la déclaration de l'entreprise. Le cocktail d'anticorps doit être administré en une seule perfusion intraveineuse dans les 10 jours suivant l'apparition des symptômes du COVID-19.
«Comme l'illustre l'action d'aujourd'hui, la FDA reste déterminée à accélérer le développement et la disponibilité de traitements potentiels contre le COVID-19 et à fournir aux patients malades un accès rapide à de nouvelles thérapies, le cas échéant, tout en soutenant la recherche pour évaluer plus avant si elles sont sûres et efficace », a déclaré le commissaire de la FDA Stephen M. Hahn, MD, dans un communiqué de presse du 9 novembre. «Grâce à notre programme d'accélération du traitement des coronavirus, la FDA continue de travailler 24 heures sur 24 et d'utiliser tous les outils à notre disposition pour ces efforts.»
La nouvelle d’Eli Lilly a été annoncée le même jour que Pfizer a déclaré qu’elle avait obtenu des premiers résultats positifs de son essai de vaccin de phase 3. Mais Pfizer a déclaré dans un communiqué que même avec un EUA approuvé, il ne serait pas en mesure de fournir l'essentiel de ses doses disponibles avant 2021.
Eli Lilly a déclaré qu'il prévoyait de fabriquer jusqu'à un million de doses de bamlanivimab d'ici la fin de 2020.
Patrizia Cavazzoni, MD
«L’autorisation d’urgence du bamlanivimab par la FDA offre aux professionnels de la santé en première ligne de cette pandémie un autre outil potentiel dans le traitement des patients atteints de COVID-19».
- Patrizia Cavazzoni, MDQu'est-ce que Bamlanivimab?
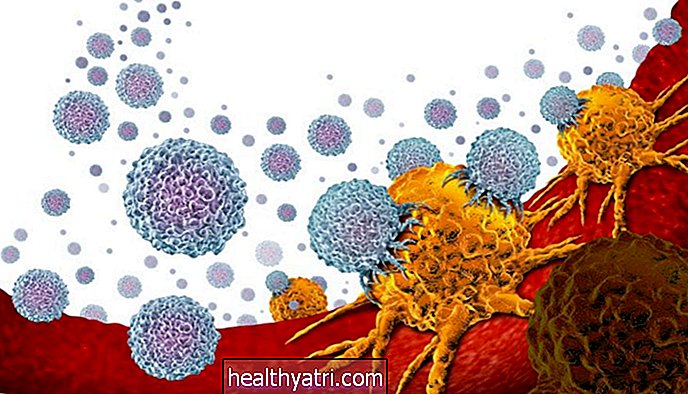
Le nom peut être difficile à prononcer, mais le but de ces anticorps est simple: «[Les] protéines de laboratoire imitent la capacité du système immunitaire à combattre les antigènes nocifs tels que les virus», a déclaré la FDA dans sa publication sur le bamlanivimab.
Fondamentalement, le bamlanivimab est un cocktail d'anticorps qui vise les protéines COVID-19, ce qui lui permet d'empêcher le virus de se fixer et de pénétrer dans les cellules humaines.
«L'autorisation d'urgence du bamlanivimab par la FDA fournit aux professionnels de la santé en première ligne de cette pandémie un autre outil potentiel dans le traitement des patients COVID-19», a déclaré Patrizia Cavazzoni, MD, directrice par intérim du Center for Drug Evaluation and Research de la FDA. Libération. «Nous continuerons d'évaluer les nouvelles données sur l'innocuité et l'efficacité du bamlanivimab dès qu'elles seront disponibles.»
Le Bamlanivimab de Lilly et le REGN-COV2 de Regeneron, le cocktail d'anticorps que le président Trump a reçu lorsqu'il a reçu un diagnostic de COVID-19, sont toujours en cours d'examen. REGN-COV2, cependant, n'a pas encore reçu d'EUA de la FDA.
Quelle est la différence entre une EUA et une approbation?
Un EUA ne doit pas être confondu avec l'approbation de la FDA.
«Pour déterminer s'il faut délivrer une EUA, la FDA évalue les preuves disponibles et équilibre soigneusement tous les risques connus ou potentiels avec les avantages connus ou potentiels du produit à utiliser en cas d'urgence», a déclaré la FDA dans sa déclaration sur le bamlanivimab. «Sur la base de l'examen de la FDA de la totalité des preuves scientifiques disponibles, l'agence a déterminé qu'il est raisonnable de croire que le bamlanivimab peut être efficace dans le traitement des patients non hospitalisés atteints de COVID-19 léger ou modéré.»
Dans le cas d'une EUA, «les avantages connus et potentiels l'emportent sur les risques connus et potentiels du médicament.»
Et après?
Le gouvernement américain a acheté 300000 doses de bamlanivimab qui, selon le communiqué de presse d'Eli Lilly, seront gratuites pour les Américains (à l'exception des établissements de santé qui peuvent facturer l'administration du médicament).