
Gracieuseté de Lucira
Points clés à retenir
- La FDA a autorisé le premier kit de test à domicile pour COVID-19.
- Les résultats sont disponibles en aussi peu que 30 minutes.
- Les experts disent que c'est une bonne prochaine étape dans l'expansion des tests.
La Food and Drug Administration (FDA) a accordé cette semaine une autorisation d'utilisation d'urgence pour le premier kit de test auto-administré à domicile pour COVID-19.
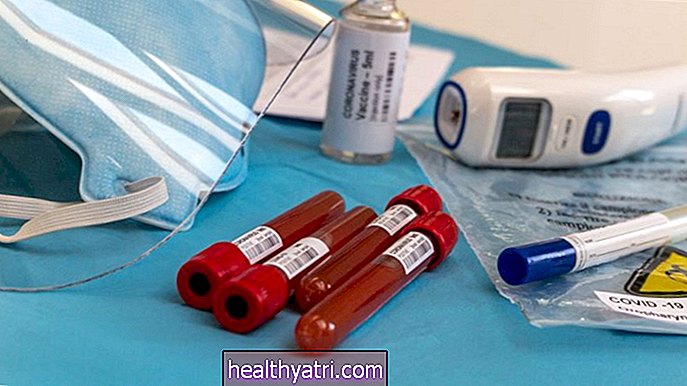
Le test à 50 $, appelé kit de test Lucira COVID-19 All-In-One, est conçu pour détecter la présence du SARS-CoV-2, le virus qui cause le COVID-19. Il est disponible pour un usage domestique pour les personnes de 14 ans et plus sur ordonnance, selon la FDA
«Bien que les tests de diagnostic COVID-19 aient été autorisés pour la collecte à domicile, c'est le premier qui peut être entièrement auto-administré et fournir des résultats à domicile», a déclaré le commissaire de la FDA Stephen Hahn, MD, dans un communiqué. La nouvelle option de dépistage est une avancée importante dans le diagnostic pour faire face à la pandémie et réduire le fardeau public de la transmission de la maladie. »
Il a ajouté: «L’action d’aujourd’hui souligne l’engagement continu de la FDA à élargir l’accès aux tests COVID-19.»
Ce que cela signifie pour vous
Vous pouvez maintenant tester le COVID-19 à la maison. Le kit de test à domicile de Lucira n'est peut-être pas encore largement disponible, mais si vous souhaitez le prendre, contactez votre médecin pour obtenir une ordonnance et les prochaines étapes.
Comment ça fonctionne
Le test rapide utilise une technologie d'amplification moléculaire, qui recherche des signes du matériel génétique du SRAS-CoV-2 chez les personnes soupçonnées d'avoir le virus. Il peut donner des résultats en seulement 30 minutes, selon la FDA.
Pour l'utiliser, un patient prélèvera un prélèvement de l'intérieur de son nez. Cet échantillon est ensuite mis dans un flacon placé dans l’unité de test. Les résultats peuvent être lus directement à partir de l’écran lumineux de l’appareil qui indique clairement si la personne est positive ou négative pour le COVID-19.
Selon Lucira Health, qui fabrique le kit de test, les recherches de la société ont montré que 100% des utilisateurs âgés de 14 ans et plus étaient en mesure d’utiliser et d’administrer le kit.
Quelle est la précision du test?
Le test a une précision comparable aux tests rapides. Lucira dit que, par rapport à un test de sensibilité autorisé par la FDA pour le SRAS-CoV-2, Lucira avait une concordance positive de 94% et une concordance négative de 98%. Et, lorsque les échantillons ont été exclus qui avaient de très faibles niveaux de virus qui pourraient indiquer qu'il n'y avait plus d'infection active, Lucira avait un pourcentage de concordance positif de 100%.
Actuellement, il existe deux types de tests de diagnostic: les tests moléculaires, tels que les tests RT-PCR, qui détectent le matériel génétique du virus, et les tests antigéniques qui détectent des protéines spécifiques du virus. Ce kit utilise un test moléculaire, qui est plus fiable que les tests d'antigène qui "fournissent généralement des résultats diagnostiquant une infection à coronavirus active plus rapidement que les tests moléculaires, mais ont une plus grande chance de manquer une infection active", selon la FDA
La FDA insiste sur le fait que les personnes dont le test est négatif mais qui présentent toujours des symptômes du COVID-19 devraient faire un suivi auprès de leur fournisseur de soins de santé «car des résultats négatifs n'empêchent pas un individu d'être infecté par le SRAS-CoV-2».
Ce que pensent les experts
«Nous attendions cela», a déclaré à Verywell Thomas Russo, MD, professeur et chef des maladies infectieuses à l'Université de Buffalo. "C'est fantastique."
Richard Watkins, MD, médecin spécialiste des maladies infectieuses à Akron, Ohio, et professeur de médecine interne à la Northeast Ohio Medical University, est d'accord. «C'est une bonne nouvelle car il existe toujours un besoin critique de tests supplémentaires aux États-Unis», déclare-t-il à Verywell. «Les tests sont un élément clé pour contrôler la pandémie.»
Amesh A. Adalja, MD, chercheur principal au Johns Hopkins Center for Health Security, dit à Verywell qu'il s'agit d'un «bon premier pas en avant». Mais, dit-il, ce n’est pas parfait. «C'est toujours un test coûteux qui nécessite une prescription», dit-il.
L'exigence de prescription «pourrait diminuer la disponibilité» pour le grand public qui peut ne pas vouloir passer par les étapes consistant à contacter son médecin et à récupérer une ordonnance avant d'être testé, dit Russo.
Il craint également que le test ne provoque une fausse confiance chez les gens. «Le test est valable pour un seul moment dans le temps», dit-il. "Mais aucun test n'est parfait, et ce que vous faites par la suite compte aussi."
Étant donné que le test n'est pas bon marché, Adalja dit qu'il peut être mieux utilisé dans des domaines comme les maisons de retraite médicalisés où des résultats rapides sont nécessaires. Il peut également gagner en popularité pour une utilisation à domicile par le grand public, mais, souligne-t-il, le coût peut être un élément dissuasif pour une utilisation régulière. Mais Watkins dit que cela peut simplement être une bonne option que les gens peuvent utiliser de temps en temps. «Cela pourrait rassurer les gens qui voyagent ou en visitent d'autres pour les vacances à venir», dit-il.
Le kit de test Lucira devrait être disponible pour les patients desservis par Sutter Health en Californie du Nord et la Cleveland Clinic Florida à Miami-Ft. Lauderdale, bientôt Au début du printemps 2021, la société s'attend à ce qu'il soit disponible à l'échelle nationale par le biais de prestataires de soins de santé.
Adalja souligne que, bien que ce soit une bonne option, les tests aux États-Unis doivent encore changer. «Il s'agit d'une première étape vers un meilleur accès aux tests, mais la technologie doit devenir moins chère et plus simple», dit-il. «Dans l'ensemble, cependant, cela indique que le paradigme est en train de changer.»


















-needed.jpg)




