Ellen Lindner / Verywell
Points clés à retenir
- Deux vaccins à base d'ARNm ont reçu une désignation accélérée de la FDA.
- Alors que le statut accéléré accélérera le développement et le processus d'approbation potentiel, Pfizer et BioNTech ont refusé tout financement fédéral pour un vaccin COVID-19.
- Si les essais cliniques réussissent, les doses initiales pourraient être prêtes d'ici la fin de l'année.
Pfizer et BioNTech ont annoncé lundi que deux de leurs candidats vaccins contre le coronavirus ont reçu la désignation «accélérée» de la Food and Drug Administration (FDA).
Pfizer, une société pharmaceutique américaine, et BioNTech, une société de biotechnologie allemande, se sont associées en mars pour rechercher des vaccins contre le SRAS-CoV-2, le virus responsable du COVID-19. ARN messager (ARNm), une méthode sur laquelle le couple travaille ensemble pour les vaccins antigrippaux depuis 2018.
Vaccins COVID-19: Restez à jour sur les vaccins disponibles, qui peut les obtenir et leur sécurité.
Que signifie Fast Track?
Le processus accéléré de la FDA facilite le développement et l'examen accélérés de médicaments - ou vaccins - destinés «à traiter des conditions graves et à« répondre à un besoin médical non satisfait ».
Plusieurs médicaments reçoivent une désignation accélérée chaque année. En juin, 20 médicaments ont été approuvés pour une procédure accélérée en 2020, en cours de développement pour des conditions allant du cancer du sein métastatique triple négatif à la maladie de la thyroïde oculaire.
Les sociétés pharmaceutiques doivent être celles qui demandent une désignation accélérée. Si elle est approuvée, la société pharmaceutique peut s'attendre à des réunions, une communication et un soutien plus fréquents de la FDA, ainsi qu'à une éligibilité à une approbation accélérée et à un examen prioritaire.
En arrière-plan, un porte-parole de la FDA a déclaré à Verywell qu'il était interdit à l'organisation de divulguer les informations contenues dans une demande de nouveau médicament expérimental, de sorte que peu d'informations publiques sont disponibles sur les raisons pour lesquelles ces candidats particuliers ont été choisis. Cependant, un communiqué de presse publié par Pfizer et BioNTech indique que la désignation accélérée a suivi "les données préliminaires des études de phase 1/2 qui sont actuellement en cours aux États-Unis et en Allemagne ainsi que des études d'immunogénicité animale."
Fast track aidera Pfizer et BioNTech dans leur objectif de fabriquer jusqu'à 100 millions de doses de vaccin d'ici la fin de 2020, en attendant les résultats des études en cours et l'approbation réglementaire. Après cela, ils fabriqueront potentiellement plus de 1,2 milliard de doses d'ici la fin de 2021.
Qu'en est-il des autres vaccins bénéficiant d'un financement américain?
Pfizer et BioNTech ne figurent notamment pas sur la liste des candidats vaccins recevant un financement du gouvernement américain, qui comprend des noms comme AstraZeneca, Moderna et Johnson & Johnson. 19 vaccins, le président-directeur général de Pfizer, Albert Bourla, a déclaré avoir refusé le financement fédéral afin d'aller plus vite.
"Lorsque vous prenez de l'argent, les gens qui donnent de l'argent veulent savoir comment vous les avez dépensés et ce que vous faites exactement", a déclaré Bourla, selonIntelligence pharmaceutiquecouverture d'un briefing virtuel du Milken Institute en juin. «La vitesse était essentielle en ce moment. Je voulais m'assurer que nous donnions à nos gens l'autonomie pour aller vite et courir et être en mesure de produire un vaccin.
Comment ces vaccins fonctionneront-ils?
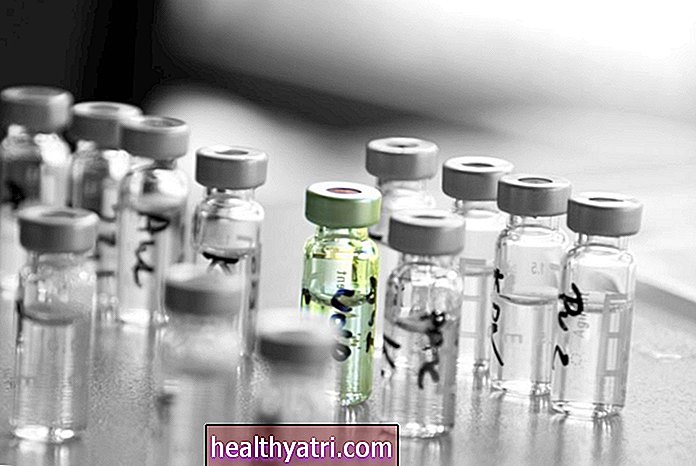
Les deux vaccins candidats, appelés BNT162b1 et BNT162b2, utilisent une plate-forme vaccinale reposant sur l'ARNm, une molécule qui aide l'ADN à fabriquer des protéines.
En théorie, l'introduction d'ARNm viral non infectieux incitera le corps à créer les protéines de pointe qui recouvrent le virus SRAS-CoV-2. À elles seules, ces pointes sont inoffensives, mais elles susciteront quand même la réponse immunitaire nécessaire pour créer des anticorps qui protègent contre le SRAS-CoV-2.
Ces dernières années, les vaccins à ARNm se sont avérés plus sûrs, plus puissants et plus efficaces à produire que d'autres types de vaccins, faisant de cette technologie une bonne option pour le milliard de doses prévues.
Pfizer et BioNTech prévoient de passer aux essais de phase 2b / 3 dès plus tard ce mois-ci avec jusqu'à 30 000 sujets.
Ce que cela signifie pour vous
La procédure accélérée signifie que si l'un des vaccins ou les deux s'avèrent sûrs et efficaces, le processus d'approbation de la FDA se déroulera plus rapidement. Cela signifie que la disponibilité des vaccins pour le grand public peut également être plus rapide.














-in-preemies.jpg)

.jpg)