Piscine / Piscine / Getty Images
Points clés à retenir
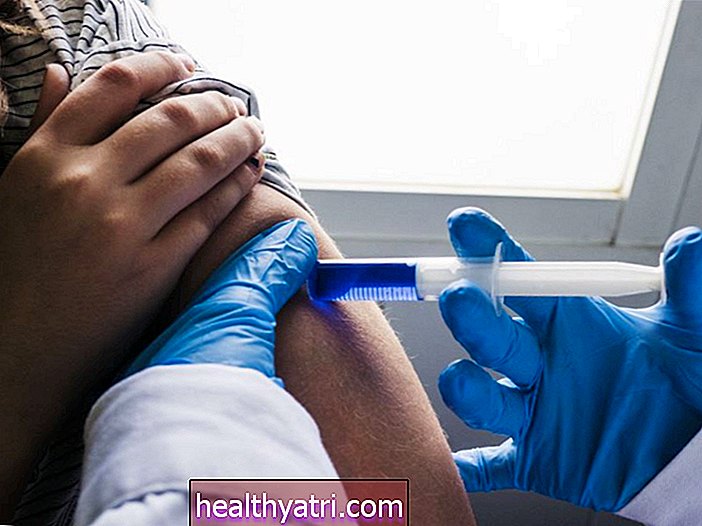
- Toute personne de 65 ans et plus est désormais éligible au vaccin
- Les personnes de moins de 65 ans qui ont un problème de santé documenté qui augmente leur risque de COVID-19 sont également éligibles.
- Le calendrier des secondes doses des vaccins actuellement disponibles - 21 jours après la première pour le vaccin Pfizer; 28 jours après le premier pour le vaccin Moderna - restent les mêmes.
- Les États devront ajouter des sites et du personnel de santé pour administrer les doses supplémentaires que le gouvernement fédéral publiera. Vérifiez auprès de votre médecin, de votre service de santé local ou appelez le 311 pour savoir où les vaccins sont disponibles dans votre région.
Lors d'un point de presse le mardi 12 janvier, le secrétaire sortant de la Santé et des Services sociaux (HHS) Alex Azar a formulé de nouvelles recommandations pour faire vacciner plus d'Américains plus tôt contre le COVID-19.
Les nouvelles recommandations rendront les doses de vaccin plus facilement accessibles à un plus grand groupe d'Américains:
- Tout le monde de 65 ans et plus
- Les personnes de moins de 65 ans souffrant de maladies chroniques documentées telles que l'hypertension artérielle, le cancer, les maladies pulmonaires chroniques. et les maladies cardiaques.
Avant l'annonce, la plupart des États suivaient les recommandations du Comité consultatif sur les pratiques d'immunisation (ACIP) des Centers for Disease Control and Prevention de ne vacciner que les agents de santé et les résidents des établissements de soins de longue durée pendant la phase de distribution initiale. À la suite de ce changement, les sites de vaccination seront élargis pour inclure de grands lieux publics et davantage de pharmacies au détail.
Au lieu de retenir les doses pour être sûr que ceux qui ont reçu une première vaccination peuvent recevoir leur deuxième dose à temps, le gouvernement fédéral prévoit maintenant de distribuer la plupart des doses de vaccin disponibles aux États.
«Toute dose de vaccin dans un entrepôt pourrait signifier une hospitalisation ou un décès de plus», a déclaré Azar lors du briefing. Lundi, selon les Centers for Disease Control and Prevention (CDC), un peu plus de 10 millions de personnes ont reçu au moins une dose d'un vaccin COVID-19.
Le directeur du CDC, Robert Redfield, MD, a déclaré que les nouvelles directives sont conformes à la planification précédente et que le gouvernement n'avait jamais prévu qu'une phase de vaccination se termine avant d'en commencer une autre.
Aucun changement prévu pour le calendrier de dosage
Lors de la conférence de presse, le secrétaire Azar a déclaré qu'aucun changement n'est recommandé concernant le calendrier des secondes doses. La recommandation continue d'être basée sur l'étiquetage en vertu de l'autorisation d'utilisation d'urgence de la Food and Drug Administration pour Pfizer (séparation de 21 jours entre les doses) et Moderna (séparation de 28 jours entre les doses).
Azar a déclaré que son équipe informerait le président élu Biden des nouvelles recommandations. L'équipe de transition de Biden a précédemment annoncé que le président élu parlerait des efforts visant à augmenter le taux et le rythme de la distribution et de l'administration des vaccins ce jeudi.
Les nouvelles recommandations interviennent alors que les cas et les décès continuent d'augmenter dans de nombreux États. Au 13 janvier, il y avait eu un peu plus de 379000 décès dus au COVID-19 aux États-Unis.
«C'est la bonne étape pour éviter le gaspillage et pour aider à prévenir certaines maladies graves et la mort, et aider à réduire la pression sur le système de santé», Leana Wen, MD, MSc, FAAEM, un médecin urgentiste et professeur invité de politique et de gestion de la santé à l'Université George Washington, raconte Verywell.
À la fin du briefing, Moncef Slaoui, chef de l’opération Warp Speed, le programme de développement du vaccin COVID-19 du gouvernement fédéral, a également informé les journalistes du rythme des vaccinations contre le COVID-19 encore en cours d'essais cliniques:
- AstraZeneca: Devrait demander une autorisation d'utilisation d'urgence début mars.
- Novavax: recrute toujours pour des essais cliniques. Résultats attendus fin mars / début avril.
- Sanofi: Début des essais cliniques de phase 2b à la mi-février
Ce que cela signifie pour vous
De nombreux États ont maintenant des sites Web d'enregistrement pour les vaccins COVID-19. Effectuez une recherche en ligne ou appelez le 311 pour savoir comment vous inscrire, surtout maintenant que davantage de personnes sont admissibles au vaccin.










-for-osteoarthritis.jpg)