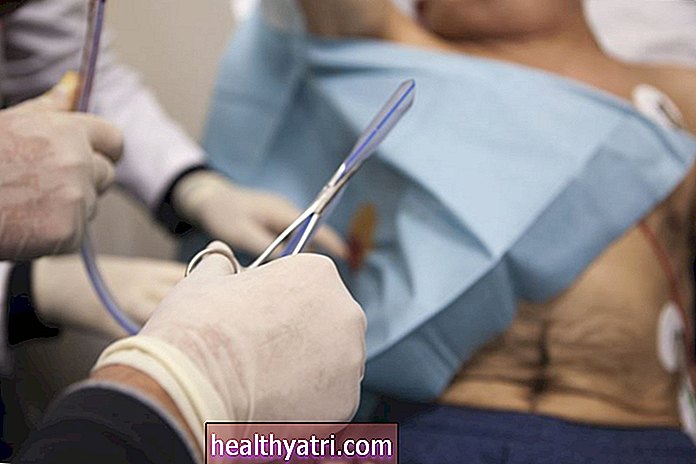
Alors que certains fabricants de vaccins utilisent de nouvelles approches pour lutter contre la maladie à coronavirus 2019 (COVID-19), d'autres se tournent vers des méthodes plus établies pour mettre fin à la pandémie.
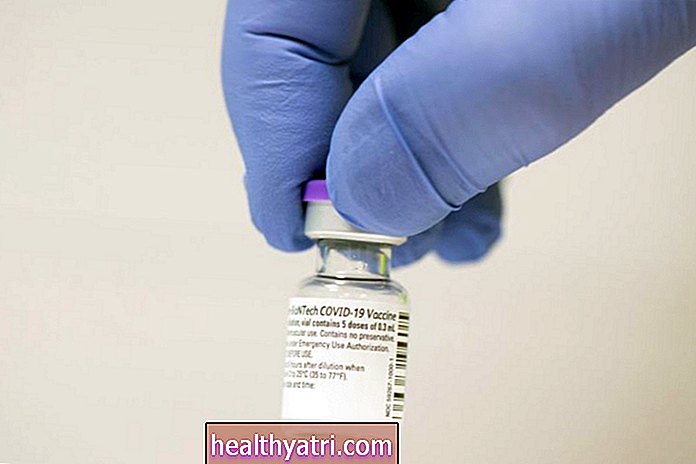
AstraZeneca et l'Université d'Oxford ont travaillé sur un vaccin à base d'adénovirus, ChAdOx1 nCoV-19 (AZD1222). Le vaccin est un vaccin à vecteur viral qui utilise un adénovirus modifié - le virus qui cause le rhume - qui contient du matériel génétique du virus SRAS-CoV-2. Le vaccin a été développé rapidement puisque cette technologie vaccinale existe depuis des décennies.
Oxford avait étudié des vaccins à base d'adénovirus pour un certain nombre d'autres maladies comme le virus Zika lorsque le COVID-19 est apparu. Les chercheurs ont adapté un adénovirus de chimpanzé affaibli pour développer le vaccin, et un essai de phase 1 a commencé en avril 2020, avec plus de 1000 vaccinations administrées au Royaume-Uni.
Les résultats initiaux de l'essai de phase 3 ont été publiés début décembre et ont examiné l'efficacité du vaccin chez plus de 11 000 des près de 24 000 personnes de plus de 18 ans inscrites dans quatre groupes d'essais au Royaume-Uni, au Brésil et en Afrique du Sud.
Il y a eu une certaine controverse autour de ce vaccin, avec des écarts de dosage dans certains groupes d'étude et une décision de la Food and Drug Administration (FDA) des États-Unis de suspendre l'essai américain en raison d'une maladie inexpliquée. La FDA a relancé l'essai après avoir examiné les données de sécurité.
Aucune audience n'est encore prévue sur une autorisation d'utilisation d'urgence de la FDA, et l'essai clinique américain devrait durer jusqu'en septembre 2021.
zoranm / Getty ImagesComment ça fonctionne
Le vaccin AstraZeneca-Oxford est un vaccin à vecteur adénoviral recombinant. Les vaccins recombinants utilisent un petit morceau de matériel génétique d'un pathogène, comme le SRAS-CoV-2, pour déclencher une réponse immunitaire. Une partie spécifique du virus peut être ciblée, et les vaccins recombinants sont généralement sûrs à utiliser dans une grande population de personnes, même celles qui ont des problèmes de santé chroniques ou des personnes immunodéprimées.
Le vaccin AstraZeneca-Oxford est un vaccin contre l'adénovirus recombinant qui utilise un agent pathogène vivant affaibli. Un inconvénient des vaccins à vecteur adénoviral recombinant est que des injections de rappel peuvent être nécessaires avec le temps. Des exemples de types similaires de vaccins recombinants (qui n'utilisent pas d'agents pathogènes vivants) sont les vaccins antipneumococciques et les vaccins contre la méningococcie. Bien que les vaccins recombinants soient courants, le seul vaccin à base d'adénovirus de ce type disponible dans le commerce est un vaccin antirabique pour les animaux.
Les vaccins contre l'adénovirus peuvent poser certains problèmes en ce que l'adénovirus est si courant que le vaccin peut ne pas être aussi efficace une fois que des doses de rappel sont administrées, ou que certaines personnes peuvent déjà être immunisées contre le virus utilisé dans le vaccin.
Le vaccin AstraZeneca-Oxford a été testé en utilisant deux doses administrées à environ un mois d'intervalle. Le dosage utilisé dans les essais n'est pas clair - avec différents récits des changements de dosage découverts pour la première fois par le service de presse Reuters. Les journalistes de l'agence de presse ont reçu deux réponses différentes d'AstraZeneca et d'Oxford pour savoir si un sous-groupe du bras britannique de l'étude a reçu des demi-doses du vaccin intentionnellement ou par accident. L'écart a été découvert après la publication des résultats préliminaires.
Quelle est son efficacité?
Que ce soit par accident ou exprès, le changement de dosage semble avoir été chanceux. Selon le rapport d'essai, le vaccin AstraZeneca-Oxford est efficace à environ 70% en moyenne. Cependant, cette moyenne a été calculée après qu'un taux d'efficacité de 62% a été observé chez les personnes ayant reçu la dose complète du vaccin, contre 90% d'efficacité chez celles qui ont reçu la demi-dose. Des examens supplémentaires sont en cours, et on ne sait toujours pas pourquoi une demi-dose de vaccin aurait pu mieux fonctionner qu'une seconde dose complète.
Quand sera-t-il disponible?
Si et quand le vaccin sera disponible est une grande question. AstraZeneca avait préparé des informations sur la distribution lorsque les résultats préliminaires ont été publiés, mais les arguments sur la question de savoir si la demi-dose du vaccin était intentionnelle et une pause dans l'essai pour des raisons de sécurité peuvent avoir ralenti les progrès du vaccin. La société a déclaré que des essais sont toujours en cours dans le monde entier, mais qu'en attendant l'approbation réglementaire, jusqu'à 3 milliards de doses pourraient être disponibles en 2021. Un certain nombre de pays ont déjà commandé des doses du vaccin et l'ont autorisé pour une utilisation d'urgence.
Une fois disponible, le vaccin pourra être distribué plus facilement que certaines autres options. Plutôt que des températures extrêmement froides comme certaines autres options de vaccin, le vaccin AstraZeneca-Oxford ne nécessitera qu'une réfrigération standard et coûtera environ 3 à 4 dollars par dose.
Les Centers for Disease Control and Prevention (CDC) mènent les efforts de vaccination, et toutes les commandes du vaccin COVID-19, quel que soit le fabricant, passeront par l'agence. Le CDC supervise également la distribution des vaccins. Le Comité consultatif des CDC sur les pratiques d'immunisation (ACIP) a formulé des recommandations sur la manière de hiérarchiser les approvisionnements en vaccins. Les agents de santé et les personnes vivant dans des établissements de soins de longue durée ont été les premiers groupes prioritaires à recevoir les vaccins COVID-19 autorisés.
Selon le CDC, il y a plus de 18 millions de travailleurs de la santé aux États-Unis et environ 1,3 million d'Américains vivant dans des établissements de soins de longue durée. Chacune de ces personnes devrait recevoir deux doses de vaccins autorisés à ce jour. . Le CDC a estimé qu'il faudra plusieurs mois avant que l'offre de vaccins ne réponde à la demande. Des conseils sur qui recevra le vaccin et quand seront décidés au fur et à mesure que les fournitures seront disponibles. Les États-Unis à eux seuls ont une population d'environ 330 millions d'habitants, ce qui signifie que près de 700 millions de doses de vaccin seront nécessaires pour vacciner toute l'Amérique si d'autres vaccins suivent une dose de deux vaccins.
Les services de santé de l'État et locaux coordonnent les efforts pour distribuer les doses de vaccins au fur et à mesure de leur disponibilité. Le vaccin doit être disponible à la fois dans les cabinets médicaux et dans les magasins de détail comme les pharmacies qui administrent d'autres vaccins.
Vaccins COVID-19: Restez à jour sur les vaccins disponibles, qui peut les obtenir et leur sécurité.
Qui peut obtenir le vaccin AstraZeneca?
L'essai clinique initial du vaccin AstraZeneca-Oxford s'est concentré sur des personnes âgées de 18 à 55 ans, et de nouveaux essais avec des personnes de plus de 55 ans ont débuté en août. Il y avait eu des essais impliquant des enfants, mais ce groupe a été retiré des données des essais à la mi-décembre. AstraZeneca et Oxford n'ont fait aucune déclaration sur ce changement.
Effets secondaires et événements indésirables
En général, les effets secondaires des vaccins COVID-19 comprenaient des douleurs au bras, un gonflement et des rougeurs à l'endroit où le vaccin a été injecté. Cependant, quelques autres effets indésirables ont été signalés, dont un qui a entraîné une pause dans l'essai clinique.
Les effets indésirables sont considérés comme des réactions médicamenteuses directement causées par un vaccin, tandis qu'un effet secondaire est une réaction physique à un médicament. Le rapport préliminaire sur le vaccin publié dansThe Lancetont révélé des résultats généralement bons en termes d'effets secondaires, mais quelques effets indésirables ont été signalés.
Il y a eu trois cas de myélite transverse - une affection caractérisée par une inflammation de la moelle épinière - chez des personnes ayant reçu le vaccin.Il a été déterminé que ces maladies étaient peu susceptibles d'avoir été causées par le vaccin, selon le rapport d'essai. Un certain nombre de décès ont également été signalés dans l'étude (la plupart dans le groupe témoin), mais ces décès n'étaient pas liés au vaccin et étaient dus à des incidents comme un accident de la route et un homicide.
Financement et développement
Le vaccin a été développé grâce à un partenariat entre Oxford et AstraZeneca. Le financement de l'étude a également été fourni par le Royaume-Uni Research and Innovation, la Bill & Melinda Gates Foundation, le NIHR Oxford Biomedical Research Center et le Thames Valley and South Midland's NIHR Clinical Research Network.